您是否曾想过有这样一类疫苗,既能对抗各种致命病毒,又无需担心可能带来的副作用?答案就是——
VLPs(Virus-Like Particles)病毒样颗粒疫苗。
什么是VLPs?
VLPs是由病毒单一或多个结构蛋白自行装配而成的高度结构化的蛋白颗粒,大多数VLPs的空壳结构为二十面体或螺旋形结构,由几种特异的结构蛋白组成,它们有着和真正病毒十分相似的特征,易于被免疫系统识别,并以与真实构象相似的途径呈递病毒抗原,从而诱导强烈的免疫反应,但却不含有病毒的遗传物质,因此无法复制或引发疾病
[1]。简单地说,VLPs疫苗提供了让免疫系统"模拟演练"的机会,以便在遇到真正的病毒时能立即作出反应进行反击,并且VLPs疫苗自带佐剂效应,相当于“打游戏自带外挂”。您是否曾想过有这样一类疫苗,既能对抗各种致命病毒,又无需担心可能带来的副作用?答案就是——VLPs(Virus-Like Particles)病毒样颗粒疫苗。
VLPs作为亚单位疫苗的一种,因具有安全、高效、可实现鉴别诊断的突出优势,近年来也被认为是最有可能替代传统灭活疫苗的最佳候选疫苗形式。VLPs疫苗的制备过程一般包括以下步骤:病毒结构基因构建与克隆、宿主表达系统选择、分离纯化、分析鉴定等
[2]。
VLPs疫苗的分类
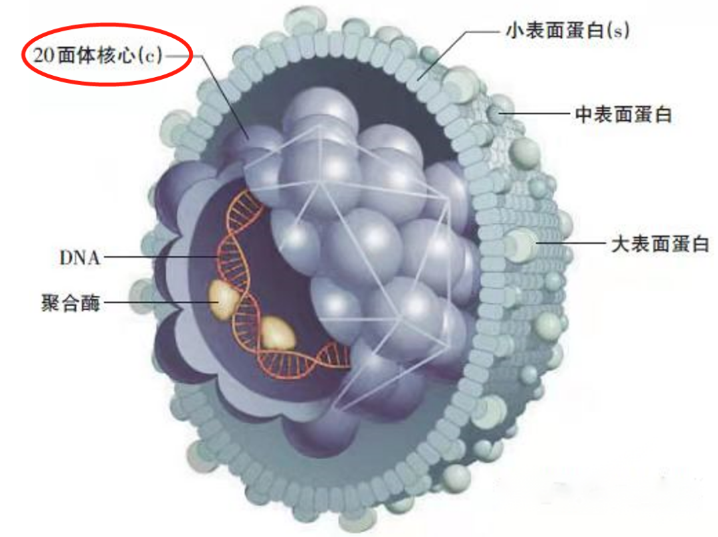
根据原始病毒的结构,VLPs疫苗可分为有包膜和无包膜两类。无包膜的VLPs疫苗只包含由病毒的蛋白形成的颗粒,如诺瓦克病毒和戊型肝炎病毒,一般由原核表达系统和低级真核表达系统实现。有包膜的病毒除了病毒本身的蛋白外,还包含宿主的细胞膜,比如A型流感病毒和乙型肝炎病毒,一般由真核表达系统实现。
图1 乙肝病毒示意图
VLPs疫苗优势在哪?
1)、安全性:VLPs不含复制酶和编码病毒结构蛋白的核酸,缺乏复制能力;
2)、高效的免疫保护力:VLPs自组装疫苗能够激活机体的免疫系统,产生特异性的抗体和细胞免疫应答,提供长期、持久的免疫保护;
3)、广泛适应性:VLPs自组装疫苗可针对不同病原体进行设计,包括病毒、细菌等,为多种传染病的预防和治疗提供了新的选择;
4)、表达系统多样性:大肠杆菌、酵母、哺乳动物细胞、昆虫细胞和植物等多种表达体系均可用于表达VLPs;
5)、稳定性和易制备性:VLPs疫苗具有良好的物理和化学稳定性,能够在极端条件下保存,容易通过工程方法大规模制备,可实现稳定的大规模生产。
这么优秀的疫苗,以前怎么没听说过?
其实不然,20世纪80年代以来,VLPs逐渐替代传统疫苗成为疫苗制备的首选
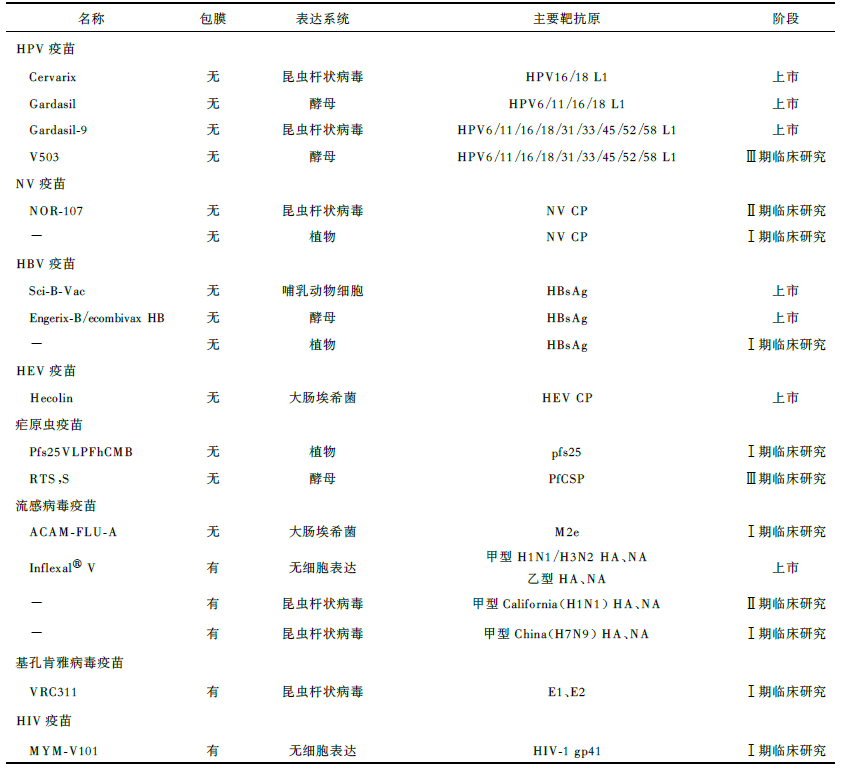
[3],并且作为炎症、疼痛、过敏、肿瘤等治疗性疫苗,早已渗透在我们的生活当中。例如乙肝疫苗、戊肝疫苗、宫颈癌疫苗和流感疫苗等都是“现役”经典的VLPs疫苗,并且由默沙东开发的乙型肝炎病毒(HBV,简称乙肝)疫苗作为全球首个VLPs疫苗早在1986年就已获批上市,随后以预防人乳头瘤病毒、戊型肝炎病毒等为适应症的预防疫苗相继上市。下图为目前上市及在研VLPs疫苗统计结果:
图2 上市及在研的VLPs疫苗
注:VLPs:病毒样颗粒;HPV:人乳头瘤病毒;NV:诺如病毒;CP:衣壳蛋白;HEV:戊型肝炎病毒;pfs25:恶性疟原虫表面蛋白25;PfCSP:恶孢子蛋白;M2e:基质蛋白2胞外结构域;HA:血凝素;NA:神经氨酸酶;E:包膜蛋白;gp41:糖蛋白41;-:未命名
VLPs疫苗的表达系统
VLPs常用表达系统包括大肠杆菌、杆状病毒/昆虫细胞、酵母及哺乳动物细胞、无细胞表达系统等,约有170种不同的宿主表达系统可用,目前已报导的VLPs疫苗约70%基于真核表达系统,30%基于原核表达系统,并且已有100余种VLPs被制备及鉴定。不同表达系统的优缺点比较见下图所示:
图3 不同表达系统比较
VLPs疫苗的纯化与组装
病毒样颗粒的纯化主要包括4个步骤,分别是裂解、粗提、浓缩和精制
[4]。
1. 裂解:当宿主表达的组装VLPs无法分泌至胞外时,纯化时需要先对细胞进行裂解
[5],哺乳动物和昆虫细胞一般采用去污剂处理,而高压、超声、研磨以及冻融等方法[6-7]则多用于细菌、酵母和植物细胞。裂解过程中最重要的是防止蛋白降解,因此需要根据蛋白质性质选择合适的缓冲体系,并添加蛋白酶抑制剂和蛋白稳定剂
[8]。
2. 粗提:这一步是将细胞碎片和大聚合物去掉
[9]。离心是蛋白粗提过程中常用的方法,一般使用低速离心机或者连续流离心机
[5]。
3. 浓缩:这一步主要的目的是去除杂蛋白和提高目的蛋白浓度。浓缩的方法有很多,包括硫酸铵沉淀、聚乙二醇沉淀、蔗糖氯化铯梯度超速离心、离子交换层析、疏水层析及亲和层析等
[10]。
4. 精纯:精制的主要目的是去除宿主自身表达的蛋白质和DNA,同时去除工艺过程引入的杂质。精纯主要采取离子交换层析、膜装置和分子排阻等方法。
5. 组装:由于不完全或者不规则的组装会导致VLPs疫苗效果的下降,因此,有时需要对VLPs进行去组装和重组装处理,以提高VLPs的稳定性、均一性和免疫原性
[11]。而且需要根据VLPs自身性质选择合适缓冲体系,例如HPV16L1 VLPs的去组装需要在高pH、低盐和还原剂的溶液下进行,重组装则需要在低pH、高盐和去还原剂的条件下进行
[9]。
病毒样颗粒的鉴定
在制备VLPs的过程中,要对VLPs的制备情况进行检测,主要通过以下4个方面:性质、含量、效果和纯度。
1. 性质:VLPs性质的检测主要包括VLPs的形态、大小、氨基酸序列、相对分子质量、降解修饰情况、中和表位、抗原特异性等方面
[12]。方法包括SDS/PAGE法、Western Blot法、ELISA法、表面等离子体共振技术、投射电子显微镜法、免疫电镜法、蛋白质测序法、质谱法等。
2. 含量:主要的方法有ELISA法、BCA法、Bradford法、紫外分光光度法等。
3. 效力:证明VLPs疫苗效果的关键,主要包括体外试验,如血凝抑制试验;体内试验,如免疫试验、攻毒试验等。
4. 纯度:检测纯化和精制效果的关键,同时也与能否用于临床试验相关。纯度检测主要检测VLPs结构蛋白的纯度、VLPs的组装率、宿主DNA和蛋白的残余、蛋白核酸复合物的多少等。主要的方法有ELISA法、SDS/PAGE法、DNA染色方法、琼脂糖凝胶电泳迟滞试验、透射电镜检测法等
[8]。
VLPs疫苗的未来
VLPs疫苗,作为一种无活性、高效率的疫苗制备方式,正在改变我们对未来免疫防御的认知。同时由于其对目标宿主细胞的天然亲和力特性已被用于如基因治疗、靶向给药等细胞靶向应用,也可与探针结合应用于生物成像或揭示病毒感染机制等基础研究当中,VLPs代表着免疫科学的前端进展,提供了一种强大且安全的工具为人类健康做贡献。


参考文献
[1] Virus-like particles in vaccine development[J]. Expert Review of Vaccines, 2010, 9(10):1149-1176.
[2] Construction and Characterization of Virus-Like Particles: A Review[J].Molecular Biotechnology, 2013, 53(1):92-107.
[3] Rational design and optimization of downstream processes of virus particles for biopharmaceutical applications: Current advances[J].Biotechnology Advances, 2011, 29(6):869-878.
[4] Recombinant expression and reconstitution of multiprotein complexes by the USER cloning method in the insect cell-baculovirus expression system.Methods, 2016, 95: 13–25.
[5] Large-scale production and purification of VLP-based vaccines[J].Journal of Invertebrate Pathology, 2011, 107(supp-S):S42-S48.
[6] Enzymatic lysis of microbial cells[J].Biotechnol Lett,2007, 29(7):985-994.
[7] Preparation of extracts from prokaryotes[J]. Methods Enzymol,1990, 182:147-153.
[8] Construction and characterization of virus-like particles:A review[J[. Mol Biotechnol, 2013, 53(1):92-107.
[9] Disassembly and reassembly of human papillomavirus virus-like particles produces more virion-like antibody reactivity[J]. Virol J, 2012, 9:52.
[10] Downstream processing of viral vectors and vaccines[J]. Gene Ther, 2005,121:103-110.
[11] Human parvovirus B19 virus-like particles:In vitro assembly and stability[J]. Biochimie, 2012, 94(3):870-878.
[12] Virus-like particle-based human vaccines:Quality assessment based on structural and functional properties[J]. Trends Biotechnol,2013, 31(11):654-663.